Оленьи рога, выращенные у лабораторных мышей в поисках регенеративной медицины — Китай
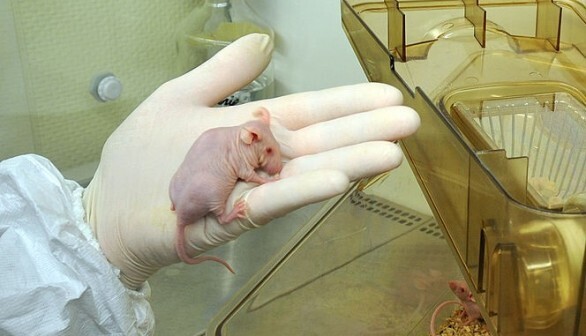
Китайские исследователи вырастили оленьи рога у лабораторных мышей в попытке продвинуть область регенеративной медицины.
Согласно недавней статье, исследователи создали "мини-рога" на мышах, введя гены оленя в геном мыши. Полученные данные свидетельствуют о том, что некоторые регенеративные гены все еще могут присутствовать у млекопитающих, которые потеряли способность к регенерации органов, и потенциально возможно использовать быстрый рост рогов для других целей.
В отличие от нынешнего клинического подхода, который в первую очередь фокусируется на лечении симптомов, регенеративная медицина направлена на восстановление тканей или органов, поврежденных болезнью, травмой или врожденными проблемами, согласно данным Института регенеративной медицины Университета Питтсбурга - Макгоуэна. Для достижения этих результатов используются тканевая инженерия, медицинские устройства, клеточная терапия и искусственные органы.
Крошечные оленьи рога для регенеративных лекарств
Рога являются одной из самых быстро регенерируемых тканей в животном мире и служат наглядным примером того, как млекопитающие могут регулярно регенерировать клетки, увеличиваясь со скоростью 2,75 сантиметра в день. Поскольку млекопитающие в целом больше не обладают способностью к регенерации органов и большинства других тканей, рога особенно интригуют. Большой придаток, который регулярно отрастает, рога обеспечивают непревзойденный обзор того, как может функционировать регенеративная медицина для костей.
Китайские исследователи Тоа Цинь и несколько его коллег глубоко изучили механизмы, лежащие в основе пантов пятнистого оленя, которые растут каждый год, прежде чем сбрасываются в поисках регенеративных лекарств. Выделив множество отдельных клеток и генов, необходимых для роста ткани пантов, они смогли создать регенеративный "атлас" пантов пятнистого оленя.
Сбрасывание рогов и лабораторных мышей
Исследователи обнаружили один тип стволовых клеток за десять дней до того, как рога были сброшены, и эти клетки сохранялись в рогах лишь короткое время после сбрасывания. Однако на пятый день после линьки появился новый подтип стволовых клеток.
После открытия различных стадий роста команда выделила стволовые клетки с наибольшим потенциалом для отрастания из сброшенных рогов пятидневной давности и старше, культивировала образцы в чашке Петри, а затем ввела их в головы мышей.
У лабораторных мышей через 45 дней появились узнаваемые мини-рога в результате того, что стволовые клетки были отнесены к категории костно-хрящевой ткани, которая является важным компонентом восстановления переломов костей. Исследователи смогли увидеть, как генетические механизмы, вызывающие развитие рогов, развиваются и как они могут быть применены в медицине костей человека, благодаря быстрому удлинению рогов.
Будущее сломанных костей
Такое лечение может вызвать этические вопросы, касающиеся имплантации клеток разных видов, а также проведения обширных испытаний на безопасность, которые будут необходимы, прежде чем его можно будет одобрить. Однако возможно, что родственные гены могут быть обнаружены у млекопитающих, если удастся обнаружить основные механизмы регенерации.
Несмотря на то, что полученные результаты нельзя полностью применить для восстановления сломанных ног, они открывают совершенно новый взгляд на то, как млекопитающие могут регенерировать ткани, как с помощью механизмов, обнаруженных в их собственных геномах, так и с помощью стволовых клеток пантов



🤔🤔🤔, Благодарю автора, за информацию.
Это всем можно будет вырастить?
Даже если всё будет ок, до широкой практики дойдёт не скоро - через десятилетия, лишь бы было ок...
Спасибо, хорошая статья. Жду новых публикаций с нетерпением.
Спасибо за публикацию!