






Хотя почти каждая клетка вашего организма содержит копию каждого из ваших генов, только небольшая часть этих генов будет экспрессироваться, или включаться. Эти активации контролируются специализированными фрагментами ДНК, называемыми энхансерами, которые действуют как искусные переключатели. Такая избирательная активация позволяет клеткам выполнять определенные функции в организме, определяя, станут ли они, например, сердечными, мышечными или мозговыми клетками.
Однако эти энхансеры не всегда включают нужные гены в нужное время, что способствует развитию таких генетических заболеваний, как рак и диабет. Группа инженеров-биомедиков из Университета Джонса Хопкинса разработала модель машинного обучения, позволяющую предсказывать, какие энхансеры играют роль в нормальном развитии и при заболеваниях, что в перспективе может стать основой для создания терапий, нацеленных на энхансеры и позволяющих лечить заболевания путем произвольного включения и выключения генов. Результаты исследования опубликованы в журнале Nature Genetics.
"Мы давно знаем, что энхансеры контролируют переходы между типами клеток, но в этой работе интересно то, что математическое моделирование показывает нам, как ими можно управлять", - сказал руководитель исследования Майкл Бир, профессор биомедицинской инженерии и генетической медицины в Университете Джона Хопкинса.
Клетки очень динамичны и изменяются в процессе нашего развития или в ответ на воздействие окружающей среды. Группа Бира была заинтересована в том, чтобы понять, как энхансеры влияют на "решения о клеточной судьбе", или процесс перехода одной клетки в другой тип клеток в ходе развития. Ошибки в принятии решений о клеточной судьбе являются одним из основных факторов развития заболеваний.
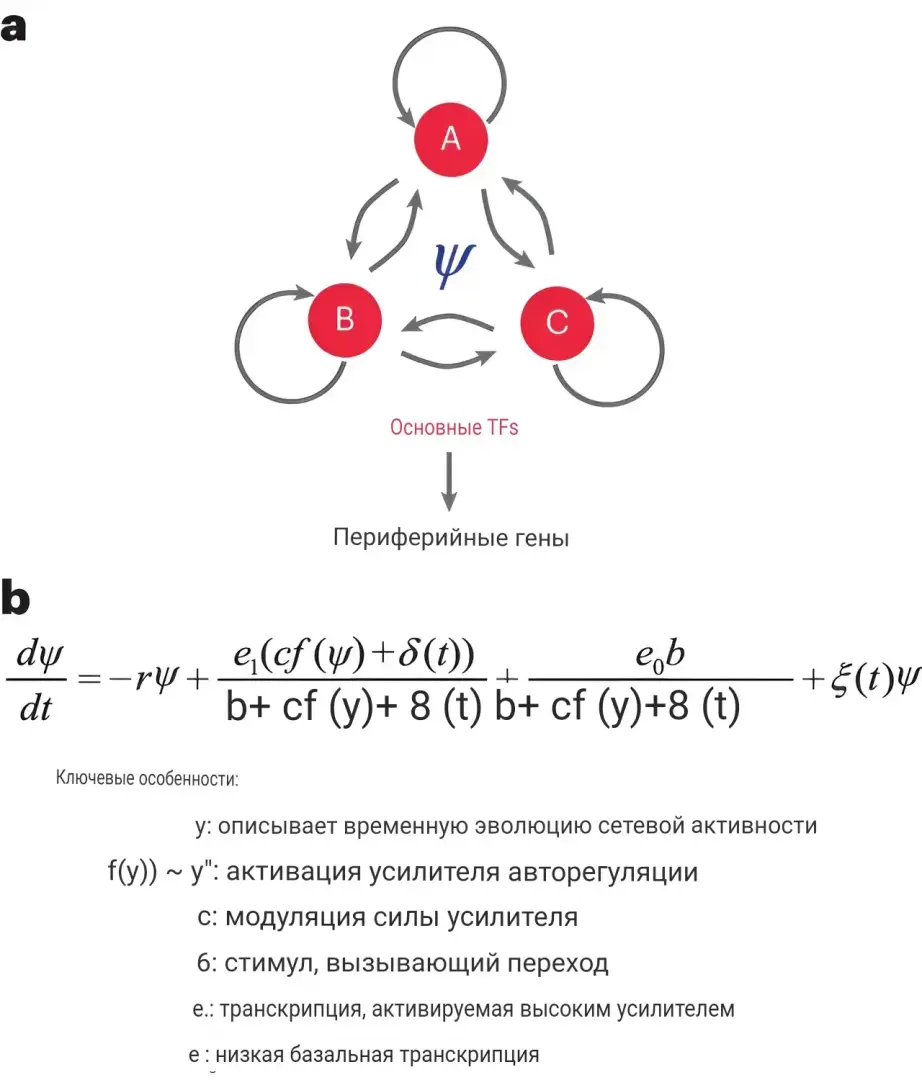
Сначала команда построила модель машинного обучения для моделирования того, как гены регулируют друг друга в клетке. Затем с помощью крупномасштабных селекционных экспериментов, известных как генетические экраны, были выявлены несколько ключевых генов, контролирующих решения о клеточной судьбе, а также энхансеры, включающие и выключающие экспрессию этих генов. Затем с помощью системы редактирования генов CRISPR были нарушены или стимулированы потенциальные энхансеры, и наблюдалось их влияние на экспрессию генов. Это также позволило исследователям проверить, какие энхансеры ускоряют переход эмбриональных стволовых клеток в эндодермальные клетки, что является первым шагом в формировании желудка или поджелудочной железы. Наконец, группа использовала данные генетического скрининга для моделирования особенностей ДНК, таких как физическая структура или модифицирующие метки, которые лучше всего предсказывают, какие энхансеры будут оказывать наибольшее влияние на судьбу клеток.
Используя этот новый вычислительный подход, команда обнаружила два удивительных свойства взаимосвязи между активностью энхансеров и судьбой клеток. Во-первых, энхансеры, оказывающие сильное влияние на экспрессию генов, находятся в петлях ДНК, окружающих ген-мишень, что позволяет получить более точную информацию о том, как геномное расположение энхансера способствует активации гена-мишени. Во-вторых, стимуляция энхансеров влияла на активацию генов только во время перехода клеток из одного типа в другой, а после завершения перехода эффект исчезал.
"Это может объяснить, почему исторически было так трудно связать варианты энхансеров с соответствующим заболеванием. Многие из этих энхансеров, ассоциированных с заболеваниями и выявленных с помощью генетики, могут существенно изменять экспрессию генов только при переходе клетки к новому типу клеток", - говорит Бир.
Полученные результаты позволяют предположить, что CRISPR-скрининги, предназначенные для обнаружения энхансеров во время перехода клетки в новое состояние, будут обладать большей чувствительностью. Команда считает, что их работа может помочь другим исследователям в изучении энхансерных мутаций, используя модели, основанные на особенностях ДНК, для предсказания того, какие из них с наибольшей вероятностью могут повлиять на судьбу клетки, а также в разработке экспериментов по выявлению труднообнаруживаемых энхансеров путем стимулирования клеточных переходов.
По мнению Бира, результаты исследования свидетельствуют о том, что судьба клетки не может быть окончательно определена, и что при дальнейших исследованиях ученые смогут определить, какие энхансеры связаны с определенными генетическими заболеваниями, что позволит им изменять функцию энхансеров для предотвращения или лечения генетических заболеваний.
"Это новый инструмент для изучения взаимодействия между генами и регуляторными элементами, такими как энхансеры, который позволит понять, как исправить аномальное поведение клеток во время болезни", - сказал Бир. "Мы ожидаем, что наша работа в будущем может послужить толчком к разработке методов лечения рака или других геномных заболеваний путем воздействия на комбинации энхансеров с помощью CRISPR".






